Die Fehlermöglichkeits- und Einflussanalyse (FMEA, auf Englisch failure modes and effects analysis) ist eine Methode des Risikomanagements. Die ISO 14971 schreibt dazu:
„Die Fehler-Möglichkeits- und -einflussanalyse (Failure Mode and Effect Analysis, FMEA) und die Analyse von Fehlermöglichkeit, -einfluss und -bedeutung (Failure Mode Effect and Criticality Analysis, FMECA) sind Techniken, durch die eine Auswirkung oder Bedeutung einzelner Bauteile systematisch festgestellt wird; sie sind geeigneter für eine ausgereiftere Konstruktion.“
Konsequent eingesetzt ist die FMEA ein wichtiges Werkzeug in der Werkzeugkiste des Medizingeräteherstellers. Man kann die FMEA in verschiedenen Bereichen einsetzen, z. B. als Prozess-FMEA (PFMEA) um Fehlermöglichkeiten in Prozessen zu bewerten oder als Design FMEA (DFMEA), um Fehler in Produkten zu erkennen und zu behandeln.
In der Entwicklung von medizinischen elektrischen Geräten wird sie in der Regel auf Modulebene eingesetzt, um Fehlermöglichkeiten zu analysieren und Maßnahmen zu definieren. Der beste Zeitpunkt zur Durchführung einer FMEA ist dabei nach der Schaltplan-Erstellung und vor dem Layout, da hier noch Änderungen einfließen können.
FMEAs werden natürlich nicht nur in der Medizintechnik eingesetzt, sondern auch im Flugzeugbau oder in der Automobilbranche. Es gibt von verschiedenen Organisationen Vorgaben und Vorschriften zur Durchführung, unter anderem befasst sich die DIN EN 60812 mit FMEAs.
Begriffe
Die folgende Tabelle zeigt wichtige Begriffe im Zusammenhang mit FMEAs.
| Deutsch | Englisch | Erklärung / Bedeutung |
|---|---|---|
| ID | ID | Eindeutige Kennzeichnung des Fehlers (z. B. Zeilennummer) |
| Komponente / Funktion | Item / Function | Die FMEA bezieht sich auf Komponenten oder auf Funktionen. |
| Möglicher Fehler / Fehlfunktion | Potential Failure Mode | Was kann für ein Fehler auftreten? |
| Fehlerursache | Failure Cause | Was ist die Ursache für den Fehler |
| Fehlerfolge | Effect of Failure | Wozu führt der Fehler (Gefährdung Patient, Anwender oder Dritte, Ausfall, … |
| Vermeidungsmaßnahme | Preventive Action | Was wird getan, damit der Fehler nicht auftritt? |
| Entdeckungsmaßnahme | Detection Action | Was wird getan, damit man den Fehler erkennt? |
| Bewertung (B) | Severity (S) | Wie groß ist die Auswirkung dieses Fehlers? |
| Auftretenswahrscheinlichkeit (A) | Occurence (O) | Wie hoch ist die Auftretenswahrscheinlichkeit? |
| Entdeckungswahrscheinlichkeit (E) | Detection (D) | Wie hoch ist die Entdeckungswahrscheinlichkeit? |
| RPZ (B x A x E) | RPN (S x O x D) | Risikoprioritätszahl |
| Empfohlene Abstellmaßnahme | Recommended Action | Was ist die empfohlene Abstellmaßnahme? |
| Umgesetzte Maßnahme | Actions taken | Was ist die umgesetzte Maßnahme? |
| Bewertung (B) | Severity (S) | Wie groß ist die Auswirkung dieses Fehlers nach der Maßnahme? |
| Auftretenswahrscheinlichkeit (A) | Occuracy (O) | Wie groß ist die Auftretenswahrscheinlichkeit dieses Fehlers nach der Maßnahme? |
| Entdeckungswahrscheinlichkeit (E) | Detection (D) | Wie groß ist die Entdeckungswahrscheinlichkeit dieses Fehlers nach der Maßnahme? |
| RPZ (B x A x E) | RPN (S x O x D) | Risikoprioritätszahl nach der Maßnahme |
Durchführung
Die FMEA wird vorbereitet und in einer Gruppe durchgeführt. Teilnehmer bei einer Design-FMEA sind HW-Entwickler und Firmware-Entwickler des Moduls, Systemarchitekt und evtl. QM-Mitarbeiter.
Die FMEA sollte vorbereitet sein. Dennoch muss genügend Zeit für die Durchführung eingeplant werden. Je nach Größe der Baugruppe kann eine FMEA von 3 Stunden bis zu mehreren Tagen dauern.
| Dipl.-Ing. Martin Bosch, Gesellschafter, Hardware-Entwickler E-Mail: bosch@medtech-ingenieur.de Tel.: +49 9131 691 241 |
|
Benötigen Sie Unterstützung bei der Entwicklung Ihres Medizingeräts? Wir helfen gerne! Die MEDtech Ingenieur GmbH bietet Hardware-Entwicklung, Software-Entwicklung, Systems Engineering, Mechanik-Entwicklung und Beratung aus einer Hand. Nehmen Sie Kontakt mit uns auf. |
|
Vorgehen
Der Ablauf der einzelnen Fehlerbetrachtungen ist in folgendem Diagramm dargestellt:
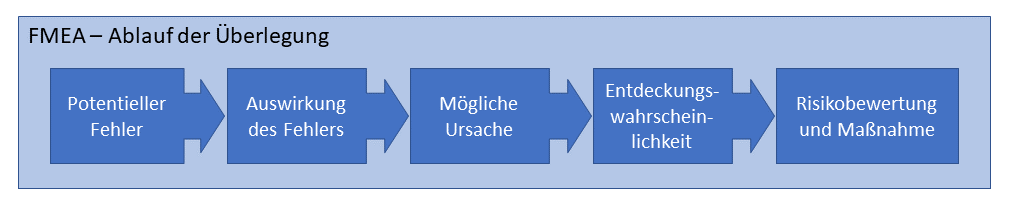
Ergebnisse einer FMEA
Bei der Durchführung einer FMEA erhält man verschiedene Ergebnisse und Erkenntnisse:
- Mögliche Fehler und Ausfallmöglichkeiten der Baugruppe oder des Systems.
- Mögliche Erstfehler, die die Sicherheit des Patienten gefährden.
- Hinweise für nötige Selbsttests oder Laufzeittests.
Die Erkenntnisse aus der FMEA können in neuen Anforderungen an das System resultieren.
Fazit
Sehen Sie die FMEA als nützliches Werkzeug, um die Qualität Ihrer Produkte zu verbessern.
Wer genauer wissen will, wie eine FMEA bei uns durchgeführt wird, kann uns gerne anschreiben oder anrufen.
Viele Grüße
Martin Bosch
Weitere Informationen zu FMEAs gibt es unter:
[1] MIL-STD-1629A
[2] Wikipedia
[3] W. W. Vandenbrande, How to use FMEA to reduce the size of your quality toolbox, Quality Progress, 1998
