Medizinprodukte haben besondere Anforderungen an die Gebrauchstauglichkeit. Denn Benutzungsfehler können bei Medizinprodukten dazu führen, dass Patienten oder Bediener einen Schaden erleiden. Um das zu vermeiden, definiert die IEC62366-1 klare Prozesse für die Gebrauchstauglichkeit von Medizinprodukten. Die Norm findet sowohl für die EU, als auch die USA Anwendung. In diesem Artikel geht es um den Annex C der Norm, der festlegt, wie mit Produkten umgegangen werden kann, für die es keine ausreichende Dokumentation der Gebrauchstauglichkeit gemäß dem Standard gibt.
Was ist eine UOUP?
Der Begriff UOUP erinnert an den Begriff SOUP („Software of unknown provenance“), der aus der Software-Entwicklung nach IEC62304 bekannt ist. Bei der UOUP handelt es sich entsprechend um ein „User Interface of unknown provenance“ oder auf Deutsch eine Benutzerschnittstelle unbekannten Ursprungs. Darunter ist ein User Interface eines Medizinproduktes gemeint, für den es keine geeigneten Aufzeichnungen gemäß der IEC62366-1 gibt.
Mit dem Annex C der Norm wird dem Hersteller ein alternativer Weg ermöglicht und es ist nicht notwendig alle Aktivitäten, die in der Gebrauchstauglichkeit gefordert sind umzusetzen. Denn die IEC62366-1 definiert das Usability Engineering als Teil des Produktentwicklungsprozesses und ist nicht dafür gedacht Produkte nachzudokumentieren! Ein User Interface gilt dann als UOUP, wenn:
- das Produkt vor 2015 entwickelt wurde und damit vor dem Erscheinen der Norm (IEC 62366-1:2015).
- das Produkt nicht als Medizinprodukt entwickelt wurde (z.B. eine Computermaus oder ein Monitor).
Sofern der Hersteller ein Produkt weiterentwickelt, dann müssen alle Änderungen nach Kapitel 5.1 bis 5.9 der Norm behandelt werden. Die nicht geänderten Teile dürfen jedoch weiter als UOUP behandelt werden.
Was ist im Falle von UOUP gefordert?
Wie bereits erwähnt, erlaubt die IEC62366-1 für UOUP einen alternativen Pfad. Ähnlich dem Vorgehen mit Legacy-Software in der IEC62304, definiert der Annex C der IEC62366-1 den Prozess und die Ergebnisse, die an UOUP gestellt werden. Dabei soll, wenn möglich, auf existierende Dokumentation aufgebaut werden, die während der Entwicklung des Legacy User Interfaces entstanden ist. Für den Hersteller ergibt sich damit die Gelegenheit keine unnötige Nachdokumentation erstellen zu müssen und sich auf das zu fokussieren, was wirklich wichtig ist. Nämlich die Gefährdungen, die sich durch schlechte Gebrauchstauglichkeit ergeben, zu erkennen und Abstellmaßnahmen zu definieren. Das Diagramm zeigt den alternativen Weg für UOUP.
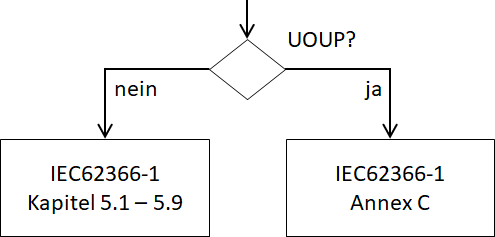
Sofern es sich um eine UOUP wie oben beschrieben handelt, sind folgende Aktivitäten gemäß der Tabelle unten notwendig.
| Aufgabe nach Annex C | Beschreibung |
|---|---|
| C.2.1 Benutzungsspezifikation (Use Specification) | Teil der Gebrauchstauglichkeitsakte (Usability Engineering File) muss die Benutzungsspezifikation (Use Specification) sein. Diese muss folgende Punkte abdecken:
|
| C.2.2 Auswertung von Post-Market-Informationen | Der Hersteller von Medizinprodukten mit UOUP soll Post-Market-Informationen (verfügbare Rückmeldungen, Reklamationen, Vorfälle und Berichte) auswerten, um ggf. bisher nicht identifizierte Gefährdungen zu identifizieren. Alle bekannten Fälle, die auf Usability zurückzuführen sind, sollen in der Gebrauchstauglichkeitsakte (Usability Engineering File) aufgeführt werden. Dabei soll insbesondere die potenzielle Schwere des Schadens bewertet werden und nicht die Anzahl der Rückmeldungen, da Benutzungsfehler oft nicht an den Hersteller gemeldet werden.
Dabei sollen insbesondere folgende Fragen berücksichtigt werden (siehe IEC TR 62366-2:2016):
|
| C.2.3 Gefährdungen und Gefährdungssituationen in Bezug auf Usability überprüfen | Der Hersteller muss die Risikoanalyse des Medizinproduktes mit UOUP überprüfen und sicherstellen, dass die mit der Gebrauchstauglichkeit verbundenen Gefährdungen und Gefährdungssituationen identifiziert und dokumentiert wurden. |
| C.2.4 Risikokontrollmaßnahmen überprüfen bzw. erweitern | Der Hersteller muss verifizieren und dokumentieren, dass angemessene Risikokontrollmaßnahmen für alle in C.2.3 identifizierten Gefährdungen und Gefährdungssituationen umgesetzt wurden und dass alle Risiken auf ein akzeptables Niveau reduziert sind, wie in der Risikobewertung angegeben. Ggf. sind Risikokontrollmaßnahmen zu ergreifen, zu dokumentieren und zu verifizieren. Sofern Änderungen an dem User Interface notwendig werden, so sind die Änderungen nicht mehr als UOUP anzusehen und für die Änderungen sind explizit die Anforderungen aus Kapitel 5.1 – 5.9 der Norm anzuwenden! |
| C.2.5 Bewertung der verbleibenden Risiken (Residual Risk Evaluation) | Der Hersteller muss das gesamte Risiko gemäß ISO 14971 neu bewerten, und das Ergebnis entweder in der Gebrauchstauglichkeitsakte (Usability Engineering File) oder in der Risikomanagementakte (Risk Management File) dokumentieren. |
Allen Herstellern von Medizinprodukten mit einer UOUP kann ich den hier beschriebenen Weg zur Gebrauchstauglichkeit ans Herz legen. Stellen Sie damit sicher, dass ihr Medizinprodukt sicher bedient werden kann und die Risiken beherrscht werden. Dann können Sie auch in Zukunft noch viel Freude mit Ihrer UOUP haben.
Falls Sie Fragen zu dem Thema haben, freue ich mich, wenn Sie uns ansprechen.
Viele Grüße
Goran Madzar
